「エピジェネティクス」と呼ばれる後成的な遺伝子発現機構とがんなどの疾患との関わりが最近の研究により明らかになりつつある。欧米のベンチャー企業を中心にこの研究成果を活用した医薬品や診断法の開発が加速しており、開発品に関する大手製薬企業との提携も出てきている。
2003年のヒトゲノム解読完了では、罹患率や病態、薬の効き方など疾患と遺伝子との関係が解明されることが期待された。しかし、実際は遺伝子配列の異常のみで説明がつく疾患はごく一部にすぎず、遺伝子配列の異常の有無以外に、エピジェネティックな異常が影響していることがわかってきた。このような背景から疾患解明や治療法開発におけるエピジェネティクスの重要性が高まっている。本稿では成長が期待されるエピジェネティック薬(epigenetic drug)の研究、開発、事業化の動向を紹介する。
1 エピジェネティクスとは
「エピジェネティクス(epigenetics) (※1)」とは、遺伝子機能の選択的な活性化・不活性化のための機構の一種で、DNAの塩基配列の変化を伴わずに細胞分裂後も継承される遺伝子機能の変化のしくみ、またはそれを研究する学問領域を指す。また、ゲノムのエピジェネティクス状態の総体を「エピゲノム(epigenome)」と呼ぶ。
ヒトの体は約60兆個の細胞から成り、個々の細胞には2万数千種類の遺伝子が記録されている。しかし、ゲノム上の個々の遺伝子発現状況(オン・オフ)は組織の種類や発生時期、外部環境などにより異なる。この遺伝子のオン・オフ制御にエピジェネティクスが関与する。具体的には、DNAのメチル化やヒストン(※2)のアセチル化、メチル化、リン酸化といった化学修飾状態が変わることで、染色体の構造が変化し遺伝子発現が調節される。これらの化学修飾は可逆的であり、外部環境や食事などにも影響されうる。エピジェネティクス情報は世代を超えて継承されるが、一卵性双生児の研究などから個体差や多様性があることが報告されている。
2 エピゲノム創薬の標的
エピジェネティクスの異常はレット症候群などの先天性疾患のほか、がん、精神疾患、生活習慣病など様々な後天性疾患と関係することが報告されている。上述のような化学修飾の状態が疾患細胞と正常細胞とでは異なることが知られている。化学修飾のなかでは特にメチル化とアセチル化に関する研究が進んでおり、これらの制御を目的とした医薬品開発を手がける企業が比較的多い。
エピジェネティクス研究の医療応用は、(1)治療薬、(2)診断法の二方面から進められている。治療薬では、がん領域の治療薬開発が活発である。細胞のがん化にはがん遺伝子の活性化と、がん抑制遺伝子の不活性化が関与することが知られている。これらの遺伝子のオン・オフに関与するエピジェネティクス関連分子が、新たな抗がん剤の標的として注目されている。代表的な標的分子はDNAメチル基転移酵素(DNMT)(※3)及びヒストン脱アセチル化酵素(HDAC)(※4)である。がん細胞で異常活性化しているこれらの酵素の働きを阻害する低分子化合物(DNMT阻害剤やHDAC阻害剤)が抗がん剤として開発されている。
診断法では、正常細胞と疾患細胞におけるDNAのメチル化状態やヒストンの修飾状態の比較データを活用した、早期診断のための診断薬キットなどが開発されている。
3 エピジェネティック薬の開発状況
3-1 上市されているエピジェネティック薬
いわゆるエピジェネティック薬はこれまで世界で4製品が承認を取得している(図表1)。日本では2製品が承認申請中である。初めて上市されたエピジェネティック薬は、米国のPharmion社(現Celgene社)が開発したDNMT阻害剤、VIDAZA(一般名:azacytidine)である。2004年に米国食品医薬品局(FDA)より骨髄異形成症候群(MDS)(※5)を適応症として製造販売承認を取得した。2009年のVIDAZA の売上高は前期比87%増の387百万ドルである。
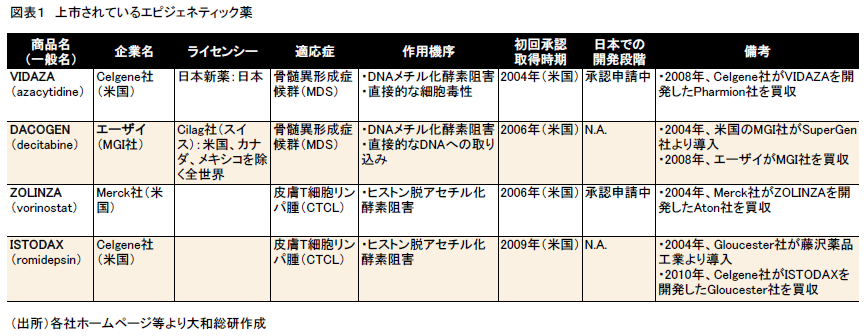
VIDAZAの日本での開発・販売権は2006年に日本新薬(株)へライセンスされており、日本新薬は2009年12月に厚生労働省に対して製造販売承認を申請した。2010年度中の承認取得を見込む。
2006年には米国のMGI社が開発したDNMT阻害剤、DACOGEN(一般名:decitabine)が米国で承認を取得した。DACOGENはVIDAZAのデオキシ類似体であり、適応症は骨髄異形成症候群である。2008年にエーザイ(株)がMGI社を買収したのに伴い、現在はエーザイが販売している。DACOGENの2009年度の売上高は前期比11%増の166百万ドル。
エーザイはDACOGENの適応拡大を進めている。米国では小児急性骨髄性白血病(AML)を適応症とした臨床試験を実施しており、2010年6月にフェーズⅢ試験の結果を発表した。2010年度中にFDAへ承認申請を行う計画である。
以上の2製品はDNMT阻害剤であるが、HDAC阻害剤ではZOLINZAとISTODAXの2製品が米国などで承認されている。
ZOLINZA(一般名:vorinostat)は米国Merck社が開発したHDAC阻害剤で、皮膚T細胞リンパ腫(CTCL)を適応症として2006年に米国で承認された。日本ではMerck社の子会社である万有製薬(株)(※6)が開発を進めおり、2010年6月に厚生労働省へ承認申請を行った。
ISTODAX(一般名:romidepsin)は、藤沢薬品工業(株)(現アステラス製薬(株))が創製したHDAC阻害剤である。2004年に米国のGloucester社が藤沢薬品工業より全世界での開発・販売権を取得。Gloucester社が開発を進め、2009年11月にFDAより承認を取得したと発表した。この直後の2009年12月、Celgene社がGloucester社を買収することを発表した。買収金額は一時金340百万ドルに加え、将来のマイルストーン達成に伴う報奨金300百万ドルとされ、合計金額は最大640百万ドルである。
3-2 関連企業
エピジェネティック薬の開発を主事業とするベンチャー企業は、欧米を中心に少なくとも20社以上存在する。図表2にその事例を示す。
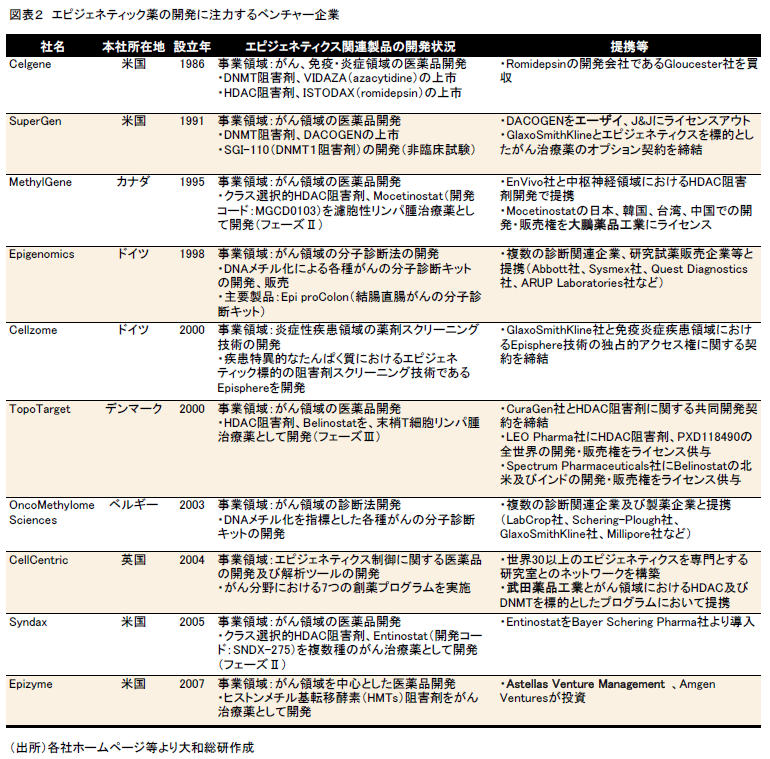
がん領域の治療薬開発に注力する企業が多く、DNMTあるいはHDACを阻害する低分子化合物が新薬候補物質として開発されている。特にHDAC阻害剤の開発を手がける企業が多い。また、DNAのメチル化やヒストンのアセチル化状態を指標としてがんの分子診断を行うキット等を開発する企業もある。
筆者が調べた範囲では日本にエピジェネティック薬の開発を主事業とするベンチャー企業は確認できなかった。
日本企業が開発を手がけるエピジェネティック薬としては、オンコリスバイオファーマ(株)が抗がん剤として開発するOBP-801(YM753)がある。OBP-801はアステラス製薬(株)が創製したHDAC阻害剤で、2009年10月にオンコリスバイオファーマが開発・販売権を取得したと発表した。契約金額は開示されていない。OBP-801は前臨床試験段階にあり、2010年中に治験申請を経て臨床試験が開始される予定である。
国内の大手製薬企業の提携事例としては、武田薬品工業(株)と英国のCellCentric社との提携が挙げられる(2010年2月、CellCentric社が発表)。これはがん領域におけるHDACとDNMTを標的とした複数のエピジェネティクス創薬プログラムに関する開発・販売権を武田へライセンスするもので、CellCentric社は対価として、一時金、開発の進捗に伴うマイルストーン報奨金、販売後のロイヤリティなど合計200百万ドル以上を武田から受け取る。武田および武田の子会社である米国のMillennium社がこれらのプログラムの非臨床試験及び臨床試験を進める。
武田はがんを重点領域に位置づけており、2008年には米国のMillennium社を約8,800百万ドルで買収している。CellCentric社との提携も一連のがん領域強化戦略の一つとみることができる。
4 今後の展望
エピジェネティクス研究の進展に加え、エピジェネティック薬の有効性及び安全性への評価が高まれば、欧米に加え日本においてもエピジェネティック薬の開発が進展する可能性が高い。
中長期的には、がん以外にも炎症性疾患や精神疾患など複数の領域でエピジェネティック薬の開発が進むことが期待される。さらに、エピジェネティクスは老化現象や、iPS細胞(※7)など各種幹細胞の性質などとも関連することが報告されており、将来的にはより幅広い医療分野で関連製品が開発される可能性がある。
ただし、エピジェネティクス制御の機構は未解明な部分が少なくない。エピゲノム創薬の進展には、ベンチャー企業や製薬企業による研究・開発と並行して、大学や研究機関における基礎研究の進展により知見が蓄積されることが重要であろう。また、DNAメチル化やヒストンのアセチル化などの修飾をより高精度・高効率に解析するための解析ツールの拡充も課題といえる。
エピジェネティクスの基礎研究は日本でも活発化しており、論文数では日本は世界の上位に位置する。これらの研究成果を活用した、日本発のエピジェネティック薬の創出に期待したい。
(※1)発生生物学者のConrad Waddington博士が1940年代に初めてこの概念を提唱したとされる。1980年代以降は分子レベルでの研究が進展し、エピジェネティクス制御の破綻ががんや精神疾患など様々な疾患と関連することが報告されている。特に2000年以降は、エピジェネティクス関連の論文数や特許出願が急増している。
(※2)真核生物のゲノムDNAに結合している一群のたんぱく質
(※3)DNAがメチル化されると遺伝子発現は抑制状態(オフ)になる。メチル化には各種のDNMTが関与する。複数種のがんにおいて、DNAの高メチル化によるがん抑制遺伝子の発現抑制が発がんに寄与することが報告されている。
(※4)ヒストンの翻訳後修飾には、アセチル化、リン酸化、メチル化、ユビキチン化などがあるが、アセチル化は転写活性化における重要性が指摘されている。ヒストンはアセチル化されるとクロマチン(DNAとヒストンたんぱく質の複合体)構造が緩み、転写因子などがDNAにアクセスしやすい状態となるため転写活性化(オン)につながるとされる。ヒストンのアセチル化レベルは、ヒストンアセチル基転移酵素(HAT)とヒストン脱アセチル化酵素(HDAC)の活性バランスで調節される。複数のがん組織で、HATの不活性化とHDACの高活性化によるヒストンの脱アセチル化が観察されている。
(※5)骨髄異形成症候群は造血器腫瘍の一種で、高い確率で白血病への移行が見られる予後不良の疾患である。患者は60歳以上の高年齢層に多く、日本新薬によれば日本での患者数は8,000人程度である。
(※6)2010年10月1日より「MSD(株)」(万有製薬とシェリング・プラウ日本法人の統合による)
(※7)人工的に多能性を誘導された幹細胞。新薬開発や再生医療などでの利用が期待されている。
このコンテンツの著作権は、株式会社大和総研に帰属します。著作権法上、転載、翻案、翻訳、要約等は、大和総研の許諾が必要です。大和総研の許諾がない転載、翻案、翻訳、要約、および法令に従わない引用等は、違法行為です。著作権侵害等の行為には、法的手続きを行うこともあります。また、掲載されている執筆者の所属・肩書きは現時点のものとなります。
同じカテゴリの最新レポート
-
地域で影響を増す外国人の社会増減
コロナ禍後の地域の人口動態
2025年07月24日
-
生成AI利活用に関する技術・サービスの動向
基盤モデルなどの最新動向、および全体像・自社事例を解説
2024年07月01日
-
コロナ禍を踏まえた人口動向
出生動向と若年女性人口の移動から見た地方圏人口の今後
2024年03月28日
関連のサービス
最新のレポート・コラム
-
消費データブック(2026/4/3号)
個社データ・業界統計・JCB消費NOWから消費動向を先取り
2026年04月03日
-
英国でもESG投資と受託者責任の関係は混迷
年金基金のESG投資に関するガイダンス策定を定める法案が否決
2026年04月03日
-
いまさら人には聞けない 大量保有報告(5%ルール)のQ&A 【改訂版】
2024年金商法等改正法(2026年5月1日適用開始)を反映
2026年04月03日
-
非財務情報は企業価値に寄与するか
非財務情報(人的資本・ガバナンス)を用いた企業価値への影響に係る定量的検証
2026年04月03日
-
生成AI時代の仕事を読む「時間差」の視点
2026年04月03日





